新闻中心
bat365中文官方网站创新药2024爆点全展望这句话出自《后汉书·窦武传》,如今苏州独墅湖畔早已布满覆辙。康宁杰瑞今日再次闪崩,不能说预料之中,但毫不奇怪。参考少数A股医药企业,闪崩体质源自深层次问题(产品结构或公司治理)没有解决。
创新药既有可预期性,又是一个概率游戏,管线年左右的窗口里,可以提前判断存在哪些节点,但能否license-out、成药或获批,始终伴随着不确定性。
明年创新药将有更高景气度,甚至泡沫化,全年爆点不断。国产1类新药接踵上市,其中部分产品将改变药企命运或行业格局;头部药企多个注册性III期临床试验揭盲,其中蕴藏着未来的药王。
在国内基础研究无法提供原创靶点的背景下,创新源头仍然在美国,但国内创新药企已越过fast-follow阶段,有了微妙的进步。
诚益生物获得1.85亿美元首付款授权给阿斯利康的GLP-1RA小分子ECC5004,是根据礼来GLP-1RA小分子LY3502970的骨架修改而来的。但这种修改不是绕过化合物专利即可,而是实现比原研分子更高的生物利用度。ECC5004 采用的 10mg 低剂量,更具便利性,提高患者依从性,并能降低制造成本。
最重要的线索藏在半年报里,公司首度承诺“坚决筛选淘汰低竞争力的 me-too 产品,力争使 First-in-class 及 Best-in-class 的高质量、差异化产品成为未来研发主体。”
恒瑞医药从前以量取胜,高景气赛道全部占位,现在质也上去了,今年10月3起海外BD授权,其中最近一起是就HRS-1167(PARP1)独家许可以及SHR-A1904(CLDN18.2 ADC)的独家选择权与德国默克达成合作,首付款高达1.6亿欧元。HRS-1167是二代PARP1,选择性更高、安全性更好。SHR-A1904是CLDN18.2 ADC,正在中国、美国、澳大利亚进行临床I期试验。
据浙商证券医药统计,2022年获批国产新药12款, 2023年1-10月获批国产1类新药(不包含疫苗及新冠治疗药物)18款药,已超2022全年数量。2024年国产新药将加速上市,恒瑞医药、康方生物大爆发。
中国企业寻找生存缝隙的能力之强,令人咋舌。当IPO通道不畅时,BD首付款竟然成为主要的输血来源。
据投行Stifel报告,在药物许可交易上,今年是中国成为医药创新净出口国的第一年,上半年对海外license-out项目的预付款(流入)是license-in项目的预付款(流出)34.9倍,而2022年这个比值为2.8倍,可谓跃迁式大进步。
2023H1中国生物尔科技 License-out交易累积达39项,总金额174亿美元,其中ADC项目交易金额近80亿美元。这背后的逻辑是分子优效设计能力的进步,并且在工程抗体(ADC、双抗)上把中国药企的改良式组合式创新禀赋体现得淋漓尽致。
最重要的结构性变化是,license-out项目由上市后阶段向临床及临床前期逐渐推进,折射着国产创新药对靶点的跟随时间点不断前置。Biotech寻求将自己的早期研发能力与跨国药企的临床开发能力、商业化能力相结合,通过BD方式对外授权仍然将是明年创新药出海的主要方式。
同时,直接出海不再有心理障碍。百济神州三季报最核心的数据是,泽布替尼美国销售额持续爬坡,2023Q3环比增长23.5%,市场份额继续扩大,与此对应的是阿斯利康阿卡替尼、艾伯维伊布替尼销售下滑。
泽布替尼的成功说明,一是生物科技领域不存在所谓脱钩阴谋论,FDA审评端和医院销售端对中国创新药没有歧视,二是头对头战胜标准疗法,被纳入美国临床诊疗指南推荐,是中国创新药海外放量最快的方式。
接下来有望出海成功创新药是百济神州替雷利珠单抗、亿帆医药艾贝格司亭α。生物类似药方面,百奥泰贝伐珠单抗、甘李药业甘精胰岛素、门冬胰岛素、赖脯胰岛素正在FDA上市审批中bat365中文官方网站。
迪哲医药舒沃替尼有望 2024 年在美国提交上市申请。亚盛医药Bcl-2APG-2575、创胜集团CLDN18.2单抗TST001是极少数自主开展全球III期临床的中国创新药。
百济神州Bcl-2Sonrotoclax(BGB-11417)联用泽布替尼进入III期阶段,头对头挑战维奈克拉联用奥妥珠单抗治疗慢性淋巴细胞白血病(CLL)。康方生物AK112(PD-1/VEGF)联合化疗头对头挑战帕博利珠单抗联合化疗一线治疗转移性鳞状非小细胞肺癌(sq-NSCLC)的国际多中心注册性III期HARMONi-3研究已完成首例患者给药。
潜在药王信达生物玛仕度肽今年底至明年上半年将有多项催化事件。玛仕度肽6mg规格的减重适应症有望向NMPA递交NDA,9mg规格有望于年底内开启减重适应症III期临床试验,6mgII期减重临床试验文章有望刊登在国际期刊bat365中文官方网站,6mgII期糖尿病临床试验文章有望刊登在国际期刊。
礼来替尔泊肽11月10日在美国获批减肥适应症(替尔泊肽减重适应症去年8月中国申报上市),适用于成年肥胖症患者和超重群体,六个剂量售价1059.87美元,预计今年底以前投放美国市场,对中国GLP-1产业链将有明显拉动,中国头部CXO承接替尔泊肽生产,蓝晓科技提供固相合成载体。替尔泊肽未获批用于减肥前已是有史以来爬坡放量速度最快的药物,二季度销售额环比激增72%。
再鼎医药艾加莫德α注射液9月5日正式在国内上市,用于治疗全身型重症肌无力患者,第一个月销售收入490万美元,显示出超强的爆发力。
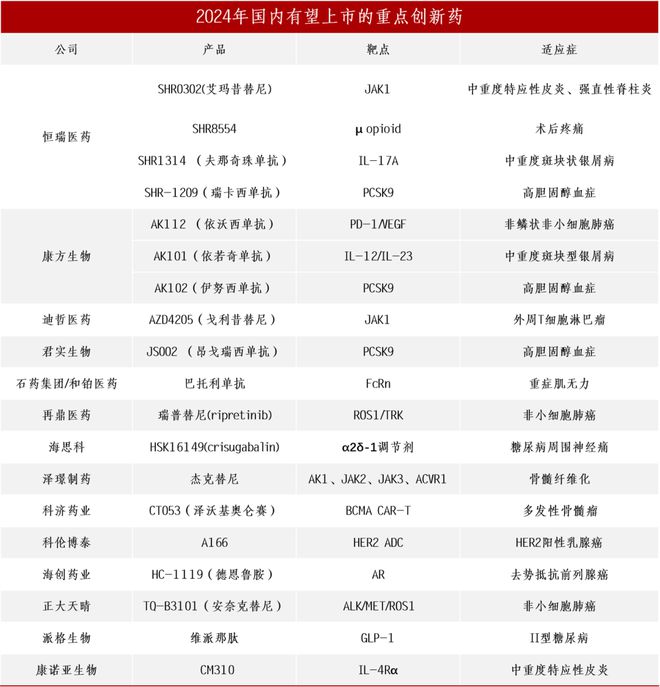
明年约有5个国产重磅自免新药上市,将彻底结束第二大疾病市场长期低迷的状况。恒瑞医药SHR0302(艾玛昔替尼) 针对中重度特应性皮炎、强直性脊柱炎,SHR1314 (夫那奇珠单抗) 针对中重度斑块状银屑病,康方生物针对AK101 (依若奇单抗) 中重度斑块型银屑病,石药集团/和铂医药巴托利单抗针对重症肌无力,康诺亚生物CM310针对中重度特应性皮炎。
自免新药将证明自己集束炸弹的力量。自免疾病之间存在共患率,一款创新药可以多个适应症,直接打开销售空间天花板。
自免检测也将被带动。国内自免检测市场主要被海外公司占据,占比达到80%,包括美国赛默飞(Phadia)、德国欧蒙bat365中文官方网站、德国胡曼、西班牙沃芬、德国 AESKU、美国伯乐。其中,德国欧蒙凭借进入市场时间最早,在国内市场占有率排名第一。目前国内企业亚辉龙、科新生物、浩欧博竞争力较强。
国内药企布局阿尔茨海默病(AD)领域的包括恒瑞医药的SHR-1707(Aβ单抗)一期临床阶段、先声制药PQ912(QPCT)二期临床阶段。
卫材/渤健Aβ单抗仑卡奈单抗2023年10月在海南博鳌乐城获批,目前已向NMPA递交了上市申请,并被纳入优先审评。
AD治疗的真正转折点是礼来Aβ单抗Donanemab,预计2024Q1获得FDA反馈,2024H1有望在美国上市。目前Donanemab在中国处于III期临床阶段。
AD诊断方面,东城药业Tau蛋白检测产品APN-1607正处于三期临床阶段,2024年有望递交NDA,与礼来合作申报的Aβ显像剂氟[18F]洛贝平注射液已于今年8月提交上市申请。考虑到目前AD诊断核药以18F标记为主,均需要依托核药房网络进行生产,因此东诚有望承接更多AD诊断核药的CDMO业务。
NASH潜在可能成功的药物靶点,主要包括GLP1、法尼醇受体(FXR)、PPAR和THR-β。THR-β激动剂Resmetirom(3期成功)及VK-2809(2期成功)验证靶点成药性,歌礼制药的同靶点药物ASC41有望获得临床成功。中国生物制药引进的PPAR激动剂Lanifibranor在国内进度最快,已推进至临床3期。国内进度较快的还有众生药业的PDE ZSP1601,作为一种全新机理化合物也已经进入临床 2b 期。

扫一扫关注bat365中文